对于气体和水体系,通过气液相平衡,我们了解到,当水和气体接触时,会出现“溶解现象”,气体分子以分子形式“溶剂化”进入水中,如果气体是氧气,就是我们常说的溶解氧了。接下来,我们来了解一下溶解了气体的水中,如何形成气泡,对于了解微纳米气泡的我们,对于加压溶解减压释放肯定不陌生,这是最常见的微纳米气泡形成方式,但是,深入了解这个过程基础理论知识的可能并不多,而实际上这个理论体系也仍在持续优化改进中,这些不断进化的理论无一例外都是从经典成核理论(Classic Nucleation theory)出发的,NANOscientific的微纳米气泡源技术中,也用到了这一基础理论的一些结论。
我们需要从热力学角度和动力学角度来了解成核过程,首先,我们来了解一下热力学成核过程。我们把过程放在P,T不变的条件下,选择最熟悉的吉布斯自由能,在生成气泡前后的变化,我们把气体、水都认为是理想的,也就是说溶解气体和水不存在溶剂化,溶解过程无焓变和体积变化。最初,水中含有大量过饱和的气体分子,但仍然认为是气体分子,因此水和气体的吉布斯自由能即化学势仍可以按照理想溶液计算,见化学势部分。系统吉布斯自由能即为两者之和,将亨利常数以溶解度形式给出:
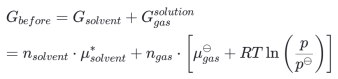
简化分析,气泡形成后系统自由能变为了四部分,水的自由能,剩余在水中饱和气体的自由能,形成的气液界面形成的表面能以及气泡内部气体的自由能,注意气泡收到拉普拉斯压力,内部压力高于外部压力,实际上水的自由能变化可以忽略:
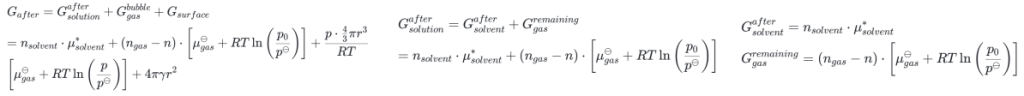
又假设气泡内部满足理想气体状态方程(实际上不满足):
p 是核胚内气体的压力
V 是核胚体积
r 是核胚半径
p0 是饱和蒸气压
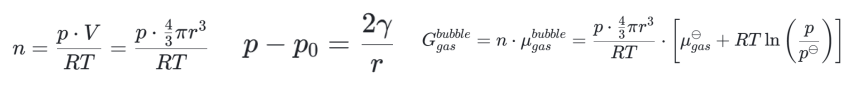
成核过程的吉布斯自由能变化 ΔG 是成核后与成核前系统吉布斯自由能的差值
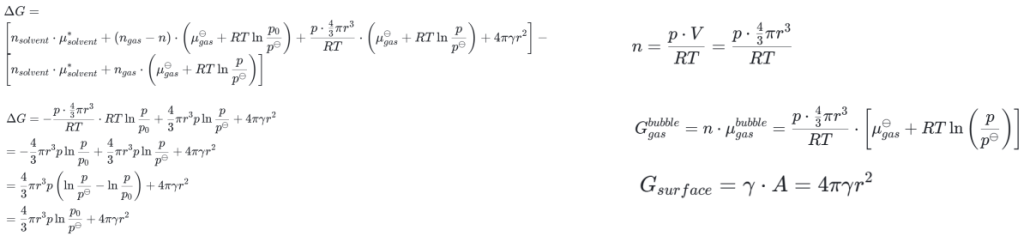
由于在平衡状态下,饱和蒸气压 p0 对应的化学势与标准态化学势关系是
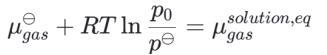
而在过饱和溶液中,气体的化学势为:
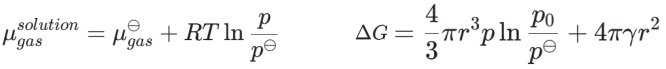
则,这一表达式描述了成核过程中吉布斯自由能变化与核胚半径 r 的关系。
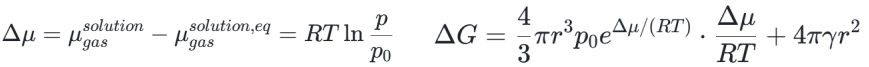
吉布斯自由能变化 ΔG 是核胚半径 r 的函数。当 r 较小时,ΔG 随 r 增大而增大;当 r 超过某一临界值后,ΔG 随 r 增大而减小。这一转折点对应的核半径称为临界核半径(r*),此时 ΔG 达到最大值,称为成核能垒(ΔG*)。求导得到,S为过饱和度。
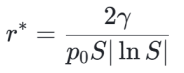
最终到了一个和关注气泡的我们有关系的公式了,这个临界变径表明,小于这个半径,吉布斯自由能随气泡变径变小而变小,气泡收缩,大于这个半径,才能成核。对于一个给定了温度压力和气体、液体的系统,如氧气和水的系统,过饱和度直接影响气泡尺寸,当过饱和度超级大时,临界半径超级小。有些做气浮的客户曾经咨询,过饱和度高,是不是对气浮可以产生更好更多的微米气泡?如果偶然看到这个公式,恰恰认证了这个说法,这是不正确的,目前,我们提及的成核过程,只是成核过程的第一阶段,即过饱和度是否可以引发成核过程,而我们工程中需要的气泡是经历成核第二阶段,即气泡生长阶段后的亚稳定微米气泡,亚稳定微米气泡的尺寸、数量和第一阶段的成核自由能变化关系并不明显,尤其在工程上,过大的饱和度会消耗非常多的能量。
我们将得到了临界半径带回自由能方程,得到成核能垒:
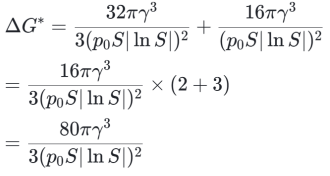
我们再看看上述成核过程的动力学,还好,到这里之前我们已经在动力学部分了解了阿伦尼乌斯方程,具有活化能(能垒)过程的动力学方程写为
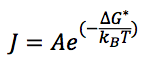
当气泡半径r>rc临界半径后,气泡在自由能的驱动下自发生长,“吸收”液体中的溶解态分子,体积膨胀,现在开始对外做体积功,同时伴随表面能变化,最终长大成为我们需要的微米级气泡。
这个过程的研究,一般都. 关键物理模型与假设液体为不可压缩、恒温体系(成核多发生在等温环境,如溶液恒温过饱和);气泡内气体视为理想气体(低压下近似成立,高压下可修正为实际气体,但核心逻辑不变);系统仅涉及体积功(忽略表面张力随体积的微小变化,聚焦膨胀做功);过饱和气体的 “过饱和度” 用压力差描述:液体中气体的溶解平衡压力为p0(饱和压力),过饱和时实际分压为P>P0,气泡内气体压力为pb,液体环境压力为pl。恒温(T不变)下系统的自由能变化用吉布斯自由能\(\Delta G\) 描述,核心公式为
![]()
气泡生长过程的自由能变化可拆分为两部分:物质转移的化学势贡献(气体分子从液体进入气泡)和气泡膨胀的体积功贡献。 气泡生长时,“外压” 即液体对气泡的压力(液体不可压缩,pl近似恒定),因此
![]()
过饱和气体分子从液体进入气泡的动力是 “化学势差”:液体中气体分子的化学势μliquid,气泡内气体分子的化学势μ bubble。
![]()
合并后,
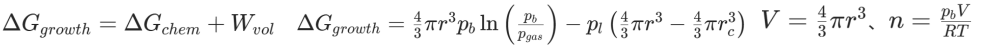
当r>rc后,气泡体积增大,第二项为负值,表示系统对外做膨胀功,导致总自由能变化中存在 “消耗能量的项”;但因为 Gchem的负向贡献(自由能降低)远大于膨胀做功的正向消耗,最终G< 0,气泡自发生长。
经典成核理论(CNT)基于一系列简化假设,这些假设在某些情况下可能不成立,导致理论预测与实验结果存在偏差。
主要局限性包括: 理想气体假设:经典成核理论假设核胚内气体为理想气体,忽略了分子间相互作用和 真实气体效应。在高压或低温条件下,这一假设可能导致显著误差。
表面张力恒定假设:理论假设表面张力 γ 是常数,不随核 胚半径变化。实际上,微小核胚的表面张力可能与宏观界面不同。
静态界面假设:理论假设核胚与周围溶液处于平衡状态,忽略了动态效应和质量传递过程。
单组分假设:经典理论通常处理单组分系统,而实际应用中多为多组分系统,组分间相互作用会影响成核过程。
连续介质假设:将核胚视为连续介质,忽略了分子离散性和统计涨落效应。
实际上,对于成核理论还有成核位点统计分布理论,但不很准确,我们就不去了解了。
